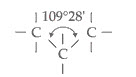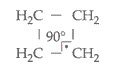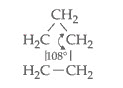Tensión Angular – Teoría de la tensión de los anillos de Bayer
Los ciclanos o cicloalcanos son hidrocarburos cíclicos saturados de fórmula general CnH2n, también conocidos como cicloparafinas
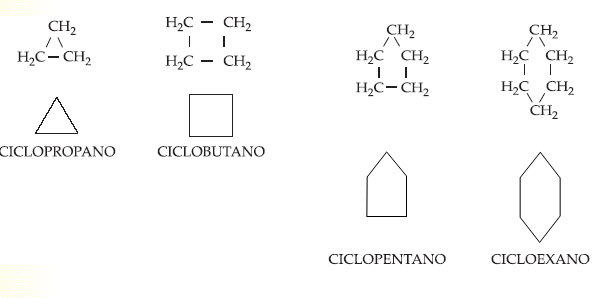
Los más importantes ciclanos son:
Propiedades Químicas de los ciclanos
Hidrogenación
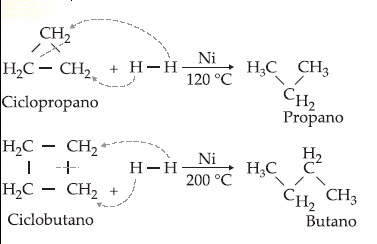
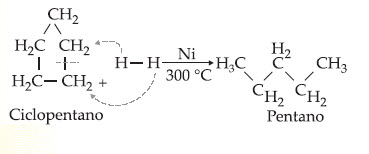
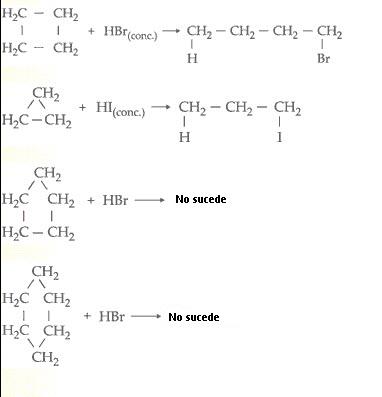
Los cíclanos con tres átomos de carbono en el ciclo adicionan hidrógeno en la presencia de níquel a temperaturas relativamente bajas (120ºC), los cíclanos con cuatro átomos de carbono en el ciclo también adicionan hidrógeno, en la presencia de níquel a temperaturas más altas (200ºC); los cíclanos con cinco átomos de carbono en el ciclo adicionan hidrógeno en la presencia de níquel a temperaturas aún más elevadas (300ºC). Los cíclanos con seis átomos de carbono en el ciclo no adicionan hidrógeno. En resumen los tres primeros cíclanos (ciclopropano, ciclobutano y ciclopentano) dan reacción de adición y los demás cíclanos, reacción de sustitución.
Por ejemplo:
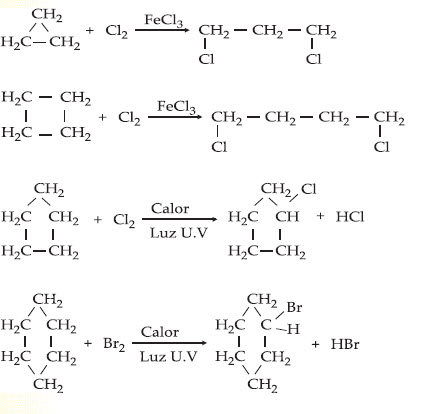
Halogenación
Reacción con Halogenhidreto (HCl, HBr, HI)
Teoría de la Tensión de los Anillos de Bayer
Por las reacciones anteriores se concluye que la estabilidad de los ciclanos aumenta desde el ciclopropano hacia el ciclohexano
Fue en 1885 que Adolf von Bayer propueso una teoría para explicar el comportameitno diferente que presentaban los ciclanos.
El ángulo formado por los enlaces simples con dos unidades de covalencia del carbono puede ser matemáticamente determinado por su valor y es de 109°28’.
Ángulo de Estabilidad Total entre los Enlaces
En un ciclo de 3 átomos de carbono, el ángulo formado entre dos unidades de covalencia es de 60°.
Existe por tanto gran tensión en el ciclo y su tendencia es la de abrirse, desde allí la facilidad con que existe reacción de adición con ruptura del ciclo.
En un ciclo con 4 átomos de carbono, el ángulo formado entre dos unidades de covalencia del carbono en el ciclo es de 90°:
En este caso la tensión es menor y la estabilidad del ciclo es mayor que el del ciclopropano. Pero la tensión del ciclobutano continúa; por tanto da a lugar la reacción de adición con ruptura del ciclo.
En un ciclo con 5 átomos de carbono, el ángulo formado entre dos unidades de covalencia del carbono en el ciclo es de 108°:
Prácticamente no existe tensión en el ciclo, de allí entonces su gran estabilidad. Sin embargo, inclusive con esa tensión mínima puede haber reacción de adición con ruptura del ciclo en condiciones enérgicas.
La teoría de Bayer no fue satisfactoria para explicar la gran estabilidad de los ciclos con seis o más átomos de carbono, porque admitía que los seis o más átomos de carbono del ciclo estaban en un mismo plano y siendo así, habría tensión en el ciclo.
Entonces, en el ciclohexano, si los seis átomos de carbono estuviesen en un mismo plano, el ángulo formado entre dos unidades de covalencia del carbono en el ciclo sería 120º y habría tensión en el ciclo, pues el ángulo normal es de 109º 28’.
A partir del ciclo de 6 átomos de carbono, a medida que aumentase el número de átomos de carbono en el ciclo, debería disminuir su estabilidad pues aumentaría la tensión lo que está en desacuerdo con la práctica porque estos ciclos son MUY ESTABLES.