Concentración de una disolución
Aunque también existan soluciones sólidas, las soluciones más comunes involucran un solvente líquido. Todos los días disolvemos substancias en agua, por ejemplo, tal como la sal de mesa o el azúcar.
Para cada conjunto de condiciones existe una cantidad límite de una dada substancia que se logra disolver en un determinado solvente y que se denomina como solubilidad de esa substancia en ese solvente.
Por ejemplo, a temperatura de 25ºC, se logran disolver cerca de 36 gramos de cloruro de sodio (sal de cocina) en 100 ml de agua, siendo por tanto la solubilidad igual a 36 g/100 ml del cloruro de sodio en agua.
Si se adiciona más sodio a la solución este no se disolverá, permaneciendo el soluto disuelto en equilibrio con respecto al sólido que está en contacto con la solución.
Es importante destacar que la solubilidad de una sustancia puede variar dependiendo de varios factores. Por ejemplo, la temperatura puede tener un gran impacto en la solubilidad. En general, la solubilidad de los sólidos en líquidos aumenta con la temperatura. Sin embargo, la solubilidad de los gases en líquidos disminuye con el aumento de la temperatura. Además, la presión también puede afectar la solubilidad, especialmente en el caso de los gases. A mayor presión, mayor será la solubilidad de un gas en un líquido.
Teniendo en cuenta la cantidad de soluto disuelto en un determinado solvente y la solubilidad de este, las soluciones pueden presentarse:
- Insaturadas: cuando la cantidad de soluto en la solución es inferior a su solubilidad
- Saturadas: si la cantidad de soluto en solución fuese igual a la solubilidad de este soluto
- Sobresaturadas: Soluciones en que la concentración del soluto en solución es superior a su solubilidad
Cuando un soluto se disuelve en un solvente, las moléculas del solvente forman estructuras en torno de las moléculas de soluto, en un proceso llamado solvatación. En el caso de las sustancias iónicas que se disuelven en solventes como el agua, el proceso de disolución implica la separación de los respectivos iones constituyentes, los cuales serán solvatados por el agua.
En estos casos, el equilibrio que se establece entre el sólido y el compuesto disuelto depende de las concentraciones en solución de todos los iones que constituyen la sal.
Para el caso del sulfato de aluminio sólido (Al2 (SO4)3) en contacto con una solución saturada de sulfato de aluminio (Al2(SO4)3 (disociado en iones Al3+ e SO42-), el equilibrio es traducido por
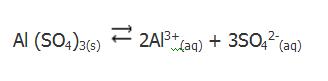
La constante que se asocia a este equilibrio se denomina Producto de solubilidad (Kps) y es expresada en el caso de esta sal, por el producto de las concentraciones molares de equilibrio de los iones cada cual elevada a los respectivos coeficientes estequiométricos.
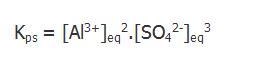
Cuando se mezclan dos soluciones pueden o no formarse precipitados. De forma de prever la formación o no de ellos, se recurre al cálculo de un cociente denominado cociente de reacción, que involucra al producto de las concentraciones de los iones involucrados a los respectivos coeficientes estequiométricos, de forma semejante a la que se utiliza para calcular el producto de la solubilidad (notemos que el producto de la solubilidad corresponde al cociente de reacción cuando la solución está saturada, o sea, cuando las concentraciones de los iones corresponden a sus concentraciones de equilibrio); se compara el valor de Q con el de Kps. Así entonces, pueden suceder tres casos diferentes:
- Si Q<Kps la solución no está saturada, entonces no existirá precipitación.
- Si Q=Kps la solución está saturada, no existiendo precipitación
- Si Q>Kps la solución está sobresaturada y hay precipitación
Cuando de la determinación del valor de Q es necesario tener en cuenta que al juntar dos soluciones, el volumen disponible para cada electrolito se altera. Siendo así es necesario calcular nuevas concentraciones de los iones intervinientes. Normalmente para este cálculo se considera que los volúmenes son aditivos.
Otro factor a tener en cuenta es la temperatura a la cual las soluciones se encuentran; si esta no fuese conocida se considera que ambas soluciones estaban inicialmente a la misma temperatura y que esta se mantiene luego de la mezcla.
Además, es importante mencionar que la concentración de una solución no solo puede expresarse en términos de la cantidad de soluto disuelto en un determinado volumen de solvente, sino también en términos de la cantidad de soluto disuelto en un determinado volumen de solución. Esta última forma de expresar la concentración es especialmente útil cuando se trabaja con soluciones diluidas, donde el volumen del soluto puede ser despreciable en comparación con el volumen del solvente.
Finalmente, cabe destacar que la concentración de una solución puede variar a lo largo del tiempo si se producen reacciones químicas en la solución. Por ejemplo, si una solución contiene un ácido y una base que reaccionan entre sí para formar agua y una sal, la concentración de los iones de la sal aumentará a medida que avance la reacción, mientras que la concentración del ácido y la base disminuirá. Este es un aspecto importante a tener en cuenta al estudiar las propiedades de las soluciones y sus cambios con el tiempo.
