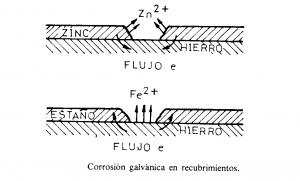
La corrosión galvánica
La corrosión del metal es la transformación de un metal o aleación de metal para su interacción química o electroquímica en medios de una determinada exposición, un proceso que resulta en la formación de productos de corrosión y liberación de energía.
Casi siempre, la corrosión metálica (para el mecanismo electroquímico) se asocia con la exposición del metal en un entorno donde existe la presencia de moléculas de agua, junto con el gas de oxígeno o iones de hidrógeno en un medio conductor.
La adopción de una o más formas de protección contra la corrosión de los metales debe tener en cuenta aspectos técnicos y económicos. Entre los aspectos técnicos, los medios de la exposición es un parámetro de gran importancia. En este parámetro, el uso de inhibidores de la corrosión o el control de los agentes agresivos (SO ² , H + , Cl – ) no son prácticos en los casos en que desee proteger un metal específico contra la corrosión atmosférica y también lo es el uso de protección cátodo, dejando a estos casos, sólo la modificación del metal o la interposición de obstáculos como una alternativa para la protección contra la corrosión.
En algunos casos, modificar el metal es perfectamente apropiado, citando como ejemplo el uso de aluminio y sus aleaciones en los componentes, tales como marcos de ventanas, puertas y ventanas en lugar de acero al carbono. Sin embargo, para grandes estructuras, en los que la resistencia mecánica es un requisito importante de aluminio y sus aleaciones no siempre puede ser usado, y los aceros inoxidables o aceros aclimatables, el potencial de materiales alternativos. El uso de los aceros inoxidables no siempre es económicamente viable, mientras que el uso de aceros aclimatables aborda la cuestión de las condiciones de exposición, ya que sólo tienen un desempeño satisfactorio en ambientes moderadamente contaminados con compuestos de azufre y en condiciones de mojado y secado, y limitación de su uso en ambientes con alta concentración de cloruro, por ejemplo, el fuerte del mar.
En resumen, hay muchos casos en los metales ferrosos (acero al carbono o hierro fundido) siguen siendo los materiales más adecuados para su uso en estructuras expuestas a ambientes en general, dejando sólo la interposición de una barrera entre el metal y el medio como una forma de protección contra la corrosión.
Con este fin, tanto recubrimientos orgánicos (pinturas) como inorgánicos (o la conversión recubrimientos metálicos, tales como anodizado, cromado) o una combinación de ambos se utilizan.
La elección de un sistema de protección contra la corrosión de los metales ferrosos (tales como acero al carbono) dependerá de varios factores, citando como una de las principales, el grado de corrosividad del medio.
En la ingeniería hidráulica y la ingeniería mecánica es una gran preocupación por la corrosión en las bombas y turbinas, principalmente debido a los daños que pueden causar las estaciones de bombeo y las centrales hidroeléctricas.
No hay que confundir el fenómeno químico de la corrosión con el fenómeno físico de la cavitación y la abrasión, a pesar de los efectos sobre las palas de la turbina y bombas son similares.