Reacción compleja
Una reacción química compleja es aquella que está compuesta por varias etapas de reacciones elementales. Una reacción compleja debe ser descrita a través de un mecanismo de reacción, que explica paso a paso las reacciones elementales que la componen.
Si una reacción química tiene al menos un compuesto intermedio, y dos etapas, ya podemos decir que es una reacción compleja.
La reacción compleja más simple sería:
A == > B == > C
Esta reacción consta de dos etapas: la primera es A == > B y la segunda B == > C, y su compuesto intermedio es B.
La mayoría de las reacciones químicas son complejas.
Existen dos características que podemos observar en una reacción, que nos indican que ésta es compleja:
* La velocidad de reacción en una reacción compleja no coincide con lo que se podría deducir de su ecuación química estequiométricamente balanceada, es decir, no está relacionada directamente con la concentración de los reactivos elevada a su coeficiente estequiométrico, sino que influyen en ella muchos otros factores.
* Se puede comprobar la presencia de compuestos intermedios entre los reactivos y los productos.
Existen distintos tipos de reacciones complejas:
* Reacciones bidireccionales: son reacciones que tienen lugar en ambos sentidos: los reactivos se transforman en productos y los productos en reactivos.
![]()
Un ejemplo de este tipo de reacción es la isomerización cis-trans del 1,2 dicloroeteno.
* Reacciones sucesivas o consecutivas: el producto de la primera etapa de la reacción es el reactivo de la segunda etapa y así sucesivamente.
A == > B == > C
* Reacciones paralelas: el reactivo es capaz de reaccionar de distintas maneras, dando lugar a diferentes productos.
A == > B
A == > C
* Reacciones en cadena: en este tipo de reacciones, los intermedios de la reacción se consumen y se regeneran continuamente.
En un proceso elemental, el número de moléculas que forman parte de los reactivos, se denomina molecularidad de la reacción. Existen reacciones elementales unimoleculares, bimoleculares, y, aunque mucho menos frecuentes, existen reacciones elementales trimolecualres.
Como ejemplo de una reacción compleja, podemos poner la descomposición del ozono, que ocurre en dos etapas, una bimolecular y otra unimolecular.
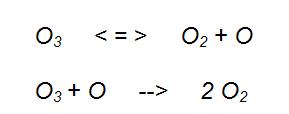
Si sumamos las dos etapas elementales, obtenemos:
![]()
Otro ejemplo de reacción compleja: la reacción de óxido nítrico y oxígeno para formar dióxido nítrico. La ecuación química global para esta reacción sería:
![]()
Sabemos que dos moléculas de NO2 no se forman por la colisión directa de dos moléculas de NO con una de oxígeno, porque se ha encontrado un intermediario en esta reacción, que es el compuesto N2O2.
Un mecanismo de reacción probable para esta reacción compleja, sería en dos etapas de reacciones elementales, como las que se describen a continuación:
Etapa 1:
![]()
Etapa 2:
![]()
Como podemos observar, la primera etapa es bimolecular, y la segunda también.
