El Cociente de Reacción
El concepto que describe el equilibrio químico en términos cuantitativos fue propuesto por los noruegos Cato Guldberg y Peter Waage en el año 1864. Ellos observaor que la concentración molar de los reactivos y productos en una reacción química en equilirio siempre obedecía a una cierta relación característica para cada tipo de reacción y dependiente apenas de la temperatura, la cual ellos denominaron constante de equilibrio.
Ellos propusieron la ley de acción de las masas para resumir sus conclusiones, cuyo enunciado es el siguiente “la velocidad de una reacción química es directamente proporcional a las concentraciones de los reactivos”. Observaron que el factor importante en la determinación de la velocidad o tasa de una reacción química no es apenas la cantidad de reactivo y si de la cantidad de reactivo por unidad de volumen.
Para un equilibrio químico en la forma de:
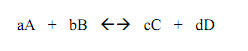
el cociente de la reacción:
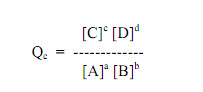
Evaluado a través de las concentraciones molares en equilibrio (simbolizadas por los paréntesis rectos [ ] ) de los reactivos y productos, es igual a una constante Kc la cual tiene un valor específico para una reacción química dada y temperatura (el subíndice c indica que la constante de equilibrio es definida en términos de concentración).
El cociente de la reacción Qc es igual a la expresión de la constante de equilibrio, sin embargo para presiones parciales o concentraciones de los reactivos y productos fuera del sistema en equilibrio.
Si Q < K entonces la reacción esta ocurriendo en dirección a la formación de los productos.
Si Q > K entonces la reacción está ocurriendo en el sentido inverso, esto es hacia los reactivos
Si Q = K la reacción está en equilibrio, utilizamos K en lugar de Q.
Por ejemplo: Una mezcla de hidrógeno (H2), Iodo (I2) y Ioduro de Hidrógeno (HI) cada uno con concentración de 0,0020 mol L-1, es introducida en un recipiente calentado a 490ºC
A esta temperatura el valor de la constante de equilibrio (K) es igual a 46 para la siguiente reacción:
![]()
Indicamos si la reacción tiene tendencia de formar más HI o no.
La solución: Calculamos el valor de Q y comparamos con K. Como K tiene un valor “intermediario” de Q, esperamos que las concentraciones de los reactivos y productos sean semejantes unas de otras. Podemos anticipar que, más allá que pueda haber una pequeña tendencia de la reacción a trasladare hacia los productos o reactivos, la extensión de la reacción será bien pequeña.
El cociente de la reacción es:
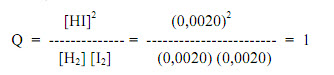
Como Q < K (K= 46), sabemos que el numerador – concentración de producto – es muy pequeña para que la composición del sistema corresponda a un estado de equilibrio.
Por tanto, la reacción tiene tendencia a continuar en dirección al lado de más formación de productos y consecuentemente asumir más reactivos.
Reglas para escribir las constantes de equilibrio:
1 – Las concentraciones o actividad de los productos son siempre colocadas en el numerador;
2 – Las concentraciones o actividades de los reactivos son siempre colocadas en el denominador.
3 – Expresar las concentraciones de los gases como presiones parciales, P, y de las especies disueltas en concentraciones molares, [ ];
4 – Las presiones parciales o concentraciones son elevadas a las potencias de los coeficientes estequiométricos de la reacción balanceada;
5 – Eliminamos los sólidos o líquidos puros y cualquier solvente de la expresión.
Nombres específicos para la constante de equilibrio:
1 – Para reacciones químicas en la fase gaseosa que utilizan presiones parciales: Kp
2 – Disociaciones del agua: constante de disociación del agua: Kw
3 – Disociación de ácidos: constante de disociación de ácidos, Ka
4 – Reacciones de base con agua: constante de disociación de bases, Kb
5 – Solubilidad de precipitados: producto de solubilidad, Ksp
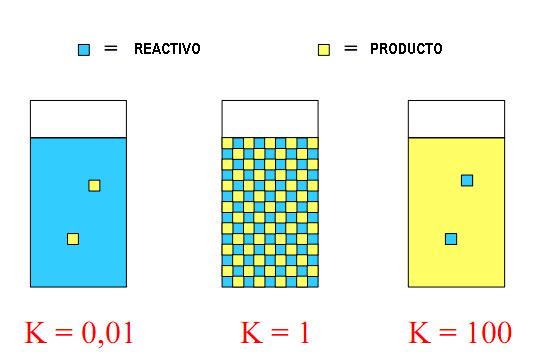
El valor de la constante de equilibrio indica la extensión con que la reacción química favorece los reactivos o los productos en el equilibrio químico.
* Valores elevados de K (mayores que 103) el equilibrio favorece fuertemente los productos;
* Valores intermedios de K (entre 10-3 y 103) reactivos y productos están presentes en el equilibrio en cantidades iguales;
* Valores pequeños de K (menores de 10-3) el equilibrio favorece fuertemente los reactivos.
La figura a continuación ejemplifica los diferentes valores de la constante de equilibrio en relación a las concentraciones de los reactivos y los productos.