Coloides hidrófilos
Un coloide es un compuesto químico en el cual coexisten dos fases, una fase dispersante y una fase dispersa (pequeñas partículas de una sustancia dispersas en otra sustancia). Cualquiera de las dos fases puede ser sólida, líquida o gaseosa, como vemos en la siguiente tabla:
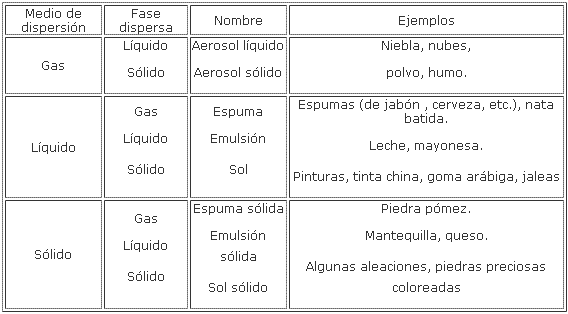
Las partículas de la fase dispersa son tan pequeñas que no pueden observarse con microscopio óptico, y suelen llamarse micelas. La afinidad de las micelas por el medio dispersante puede ser alta (liofilia) o baja (liofobia). Cuando el medio dispersante es el agua, podría hablarse de hidrofilia o hidrofobia.
Un ejemplo de coloide hidrófilo podría ser una larga cadena de hidrocarburo, con un grupo polar en un extremo, disperso en agua. Se formarían puentes de hidrógeno entre las moléculas de agua y los grupos polares del extremo, mientras que las largas cadenas apolares quedarían en el interior de la micela, sin tener contacto con el agua.
La figura a continuación representa la estructura de una micela.
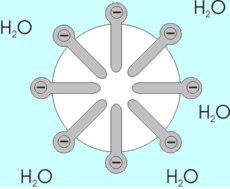
La hidratación del coloide se debe a la atracción mutua de las moléculas de agua y las micelas, dado el dipolo existente en la molécula de agua, y la carga eléctrica de la micela, las cargas de signo contrario se atraen y finalmente se unen.
Este fenómeno de fijación de agua por parte de las micelas es llamado imbibición o gelificación, y puede demostrarse introduciendo un trozo de agar o gelatina en un recipiente con agua, éste comienza a hincharse, absorbiendo agua, y adquiriendo una consistencia blanda.
Los coloides hidrófilos suelen ser reversibles, es decir, cuando causamos la precipitación de las micelas, éstas pueden volver al estado coloidal agregando dispersante nuevamente.
Presión oncótica
La presión osmótica en una verdadera solución depende de la concentración del soluto. En cambio en los coloides hidrófilos concentrados, la presión osmótica es mayor, debido a que la hidrofilia de las micelas aumenta la avidez de éstas por el agua, entonces la presión de retención es mayor, y se denomina presión oncótica. En los coloides muy diluídos, el efecto de la presión oncótica es menor, debido a la poca cantidad de micelas.
