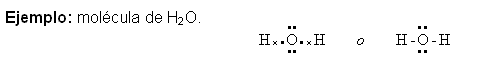Electrón de valencia
Los electrones que se encuentran en los mayores niveles de energía de determinado átomo son llamados electrones de valencia. Son los que posibilitan la reacción de un átomo con otro, del mismo elemento o de elementos diferentes, ya que tienen facilidad o predisposición para participar en los enlaces. Sólo los electrones que se encuentran en la superficie externa del átomo son capaces de interactuar con electrones de otro átomo, éstos son los electrones de valencia.
Los enlaces formados pueden ser del tipo iónico, covalente o de traslape de orbitales. En el enlace iónico los electrones de valencia son cedidos por un átomo y ganados por el que tiene mayor afinidad por los mismos. Pongamos por ejemplo el átomo de sodio, que tiene un solo electrón de valencia, y lo pierde con facilidad. Frente a un átomo de cloro, el cual tiene siete electrones de valencia y predisposición a ganar uno más y completar ocho electrones (regla del octeto) el sodio cederá el suyo, formándose un enlace iónico.
En el enlace covalente, los electrones de valencia no son cedidos ni ganados, sino que se comparten. Supongamos dos átomos de hidrógeno. Cada átomo tiene un electrón de valencia en su orbital 1s, necesitando ambos un electrón más para completar el orbital. Entonces, al reaccionar entre ellos, los orbitales 1s de ambos se solapan y los átomos pasan a compartir los electrones, y así completar los dos su orbital, formándose la molécula H2.
En los átomos que presentan varios electrones de valencia, se podrán observar varios enlaces, con el mismo átomo o con átomos distintos.
Los símbolos de Lewis o símbolos de electrón punto son una manera muy sencilla de representar los electrones de valencia de un átomo y de visualizar los que participan en enlaces y los que quedan solitarios. En este tipo de representación observamos el símbolo químico del elemento rodeado de un cierto número de puntos, que representan los electrones de valencia. El símbolo químico representaría el núcleo del átomo y los electrones internos.
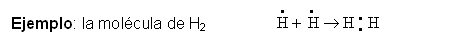
El par de electrones compartidos brinda a cada átomo de hidrógeno dos electrones adquiriendo la configuración electrónica externa del gas noble helio.
Una estructura de Lewis es la representación de un enlace covalente, donde el par de electrones compartidos se indica con líneas o como pares de puntos entre átomos. Los electrones de valencia que no participan del enlace se representan como puntos alrededor del átomo correspondiente. Solo se representan los electrones de valencia.