Teoría Del Enlace de Valencia
La teoría del enlace de valencia intenta explicar como dos átomos se enlazan entre si, buscando así presentar una interpretación satisfactoria para los enlaces covalentes.
En esta teoría lo que esta incluido es la combinación de dos orbitales atómicos de dos átomos distintos.
Siendo así, se busca estudiar y explicar como es que se da un enlace covalente. Actualmente hay diversos modelos y teorías que explican un enlace covalente, sin embargo históricamente esta fue la primer teoría en hacer esto.
Es importante recordar que esta teoría concuerda con los conceptos y teorías anteriores, aceptados hasta entonces. Una de estas teorías afirmaba que los electrones que participaban de enlaces están en la capa más externa del átomo. Se trata por tanto, de los electrones de valencia.
La pregunta ahora es, ¿como es que los electrones logran mantener dos átomos unidos?
La respuesta a esa pregunta vino de la interpretación matemática de los orbitales atómicos, que indicaban la posibilidad de combinarse formando, al final, otro orbital distinto de los anteriores y por eso no podría llamarse más orbital atómico. Así, cuando dos orbitales atómicos se combinan, el resultado final también será un orbital, sin embargo no será ya un orbital atómico.
Ejemplo: Como se da el enlace formado por la molécula más simple (H2)?
Para explicar este enlace debemos imaginar que dos átomos de hidrógeno se aproximan de forma que sobreponen sus orbitales más externos (en este caso el orbital 1s). El resultado de esta superposición corresponderá a un nuevo orbital que engloba los dos núcleos. La figura a continuación ilustra bien esta situación:

Superposición de los orbitales
Observe que los orbitales atómicos del tipo s presentan forma esférica y el resultado de la combinación de dos orbitales s genera otro orbital ovalado (un elipsoide), esa forma no es definida para ningún orbital atómico conocido.
Algunos datos pueden ser extraídos de esta figura. Si los electrones presentan la misma carga, como es que pueden mantenerse próximos uno del otro sin que exista una fuerza de repulsión intensa.
Para responder esa pregunta debemos analizar dos situaciones distintas: 1a) como eran las atracciones electroestáticas de los átomos antes del enlace; 2a) como quedarán las atracciones electroestáticas luego del enlace.
1a – Inicialmente había para cada núcleo de hidrógeno, un único electrón, así que la fuerza de atracción entre esos dos corpúsculos, a medida que se aproximaban era: el 1o Protón (p1+) atrae a su Electrón (e1–); el 2o Protón (p2+) atrae a su Electrón (e2–)., mas allá de las repulsiones de las partículas de cargas iguales. Así las interacciones serán:
p1+ ↔ e1– (atracción)
p2+ ↔ e2– (atracción)
p1+ ↔ p2+ (repulsión)
e2– ↔ e2– (repulsión)
2a – Luego del enlace, se tiene un orbital nuevo, que engloba los dos núcleos y que acomoda los dos electrones. Estos pueden estar en cualquier posición dentro del espacio delimitado por ese orbital. Aquí se puede decir que no hay mas distinción entre los electrones, porque tanto uno cuanto el otro va a poder circular libremente dentro del orbital resultante.
En este caso el electrón que originalmente vino del átomo 1, puede circular sin restricciones en torno del átomo 2 y viceversa. En este sentido decimos que los núcleos están compartiendo el par de electrones. Analicemos entonces como quedan las interacciones de atracción y repulsión entre los corpúsculos cargados eléctricamente.
p1+ ↔ e1– (atracción)
p2+ ↔ e2– (atracción)
p1+ ↔ e2– (atracción)
p2+ ↔ e1– (atracción)
p1+ ↔ p2+ (repulsión)
e1– ↔ e2– (repulsión)
Vemos que luego del enlace el núcleo del primer átomo atrae, además del suyo propio, el electrón proveniente de otro átomo, aumentando así las fuerzas de atracción electroestáticas, que van a garantizar estabilidad a la molécula, haciendo con que los núcleos permanezcan unidos.
Otro factor que garantiza que los núcleos se mantengan unidos está en que el par de electrones permanece preferencalmente entre los dos núcleos, creando un efecto conocido como efecto de blindado, porque cuando los electrones están entre los núcleos, promueven una disminución de la repulsión p1+ ↔ p2+ (entre los núcleos), una vez que crean una “barrera”, impidiendo que un núcleo perciba al otro.
Es importante recordar que en esa molécula el par de electrones no va a permanecer todo el tiempo entre los enlaces, porque el orbital que los contiene no establece esa restricción. Así, los electrones en algunos breves instantes pueden no encontrarse entre los núcleos.
Cuando un enlace se dorma en torno de un eje longitudinal de simetría, es clasificado como siendo del tipo sigma (s):

Siguiendo la teoría de enlace de valencia, un enlace covalente se forma cuando hay una superposición (y consecuente combinación) entre dos orbitales atómicos, provenientes de átomos distintos. En el ejemplo anterior fueron combinados dos orbitales iguales (s + s). ¿Será que podremos combinar otros orbitales atómicos para establecer enlaces covalentes? Veamos algunos ejemplos
Ejemplo: Como quedaría la molécula de H – F
En la molécula de HF tenemos algo diferente. El flúor tiene como configuración en su capa de valencia:
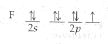
donde encontramos uno de los orbitales 2p ocupado por un único electrón. Es con ese orbital parcialmente ocupado que el orbital 1s del hidrógeno se superpone.
En este caso, el electrón de hidrógeno y un electrón de flúor se emparejan y son compartidos por los dos núcleos. Debemos notar que el orbital 1s del átomo de hidrógeno no se superpone a cualquiera de los orbitales atómicos ya completos del flúor, visto que habría entonces tres electrones en el enlace (dos del flúor y uno del orbital 1s del hidrógeno). Esa situación no es permitida. Apenas dos electrones con sus spins emparejados pueden ser compartidos por un conjunto de orbitales superpuestos.
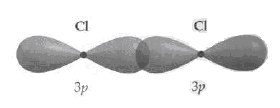
En otro caso la superposición de orbitales atómicos de átomos distintos pueden ser ambos del tipo p, como es por ejemplo en la molécula de Cl2
Enlaces Múltiples
Dos orbitales p pueden también sobreponerse uno sobre el otro, lado a lado. Cuando esto sucede el enlace resultante no tiene simetría longitudinal (o simetría axial). La figura a continuación muestra la superposición de dos orbitales p, paralelos y verticales (pz)
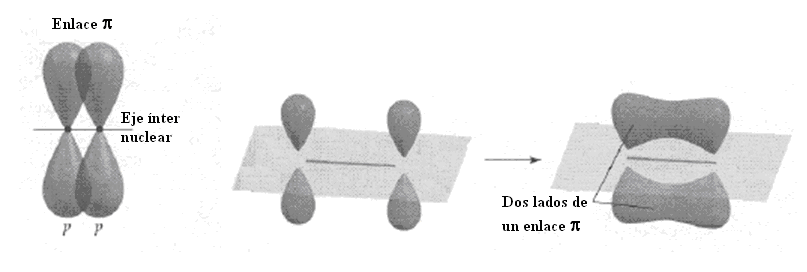
Puede verse que la superposición ocurre en dos regiones que están en lados opuestos del eje de enlace. El resultado es conocido como un enlace p (pi).
Enlace Doble: Un doble enlace consiste en un enlace s mas un enlace p, como ocurre en la molécula de O2. La combinación resultante de la combinación de orbitales 2px – 2px, indicada por un trazo en la figura anterior, representa el enlace s, ya en la superposición de los orbitales verticales (2pz – 2pz) corresponde al enlace p. Por tanto el enlace doble es constituido por los enlaces s + p.
Enlaces Triples: El triple enlace es un enlace s más dos enlaces p. La molécula de N2 es un buen ejemplo de tal enlace. La figura a continuación nos ilustra esta situación:
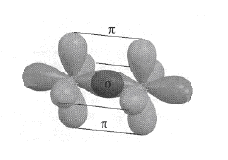
En este caso tenemos la representación de los tres orbitales atómicos p de dos átomos de nitrógeno que se enlazan a través de los enlaces s + p + p.
