Formas alotrópicas del fósforo
 En química, la alotropía es una propiedad que poseen algunos elementos químicos, al poder presentarse con distintas estructuras moleculares. Un elemento es alótropo cuando aún encontrándose en el mismo estado físico, tienen estructuras y aspectos diferentes. Las propiedades deben observarse en el mismo estado de agregación de la materia.
En química, la alotropía es una propiedad que poseen algunos elementos químicos, al poder presentarse con distintas estructuras moleculares. Un elemento es alótropo cuando aún encontrándose en el mismo estado físico, tienen estructuras y aspectos diferentes. Las propiedades deben observarse en el mismo estado de agregación de la materia.
Existen diversas formas alotrópicas muy conocidas, como por ejemplo, el ozono, el grafito o el diamante.
En este caso, trataremos las formas alotrópicas del fósforo.
El fósforo presenta una alotropía complicada, llegándose a mencionar alrededor de once formas alotrópicas diferentes, sin embargo, las más conocidas y quizás mejor caracterizadas son las conocidas con los nombres de: fósforo blanco, fósforo negro, y fósforo rojo.
Fósforo blanco:
Se forma cuando se calienta el fosfato cálcico con presencia de sílice y carbón , a una temperatura de 1400ºC, condensándose los vapores, que no son otra cosa que el fósforo blanco, P4 :
2Ca3( PO4)2 + 3 SIO2 + 10C ↔ P4 + 3 Ca2SiO4 + 10 CO
La especia P4, tiene una forma tetraédrica, como índica la figura, donde cada átomo de fósforo forma un enlace sencillo con los sus otros tres átomos vecinos, con ángulos de enlace de 60º. Loa ángulos de dichos grados se dice que se encuentran en tensión, esperándose que la molécula sea debido a esto, reactiva.
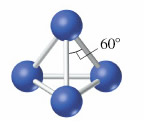
Algunas de las características más destacables son:
- El fósforo blanco, es un sólido blanco como su nombre indica, que se torna amarillo cuando se ve expuesto a la luz. Su punto de fusión es 44ºC, mientras que su punto de ebullición es de 287ºC. Por encima de los 50ºC se inflama en el aire.
- Es extremadamente venenoso y prácticamente insoluble en el agua, pero en cambio, si es soluble en benceno y CS2.
- Cuando a éste alótropo se le expone al aire, se oxida dando una llama verde y produciendose la formación de PO2, y algo de ozono.
- Produce unas reacciones bastante violentas con toda la familia de los halógenos.
- El ácido nítrico lo oxida lentamente, convirtiendolo en ácido fosfórico, y el NaOH, lo convierte en fosfina e hipofosfito sódico:
P4 + 3 NaOH + 3 H2O ↔ PH3 + 3 NaH2PO2
Este alótropo ha tenido un extenso uso militar, utilizándose como agente incendiario, para crear cortinas de humo, y como componente antipersona ya que puede producir quemaduras bastante graves, por todo esto se le conoce también como arma química. Los militares lo conocen como WP (del inglés, White phosphorus), llegándole a dar apodos durantes las guerras.
Fósforo negro:
El fósforo negro es la forma alotrópica más estable de este elemento químico. Fue preparado por primera vez, por el físico americano P.W. Bridgman.
Se obtiene a través de calentamiento del fósforo blanco cuando se encuentra a presiones elevadas.
Este alótropo recuerda al grafito en su aspecto y también en lo que se refiere a la conductividad eléctrica, pues posee una red en capas, donde cada átomo de fósforo se encuentra enlazado a otros tres átomos a una distancia de 2.20 Ǻ y con uno ángulos de enlace de 99º.
Esta forma alotrópica es cinéticamente inerte, y ni siquiera a 400ºC arde, así que mucho menos al aire.
Fósforo rojo:
El fósforo rojo se obtiene calentando el fósforo blanco, en una atmósfera inerte, a unos 250 ºC de temperatura. Es de color rojo, amorfo, y más bien poco soluble tanto en agua como en disolventes orgánicos.
La reactividad de este alótropo del fósforo es intermedia entre las otras dos formas alotrópicas. La gran diferencia de reactividad del fósforo blando y la del rojo, hace que sea interesante observar el valor del ΔHº para la conversión del fósforo rojo en blanco, siendo ésta de tan sólo 17.6 KJ.mol^-1.
De manera contraria al fósforo blanco, el rojo no es nada soluble en disulfuro de carbono y tampoco es tóxico.
Cuando se pone en contacto con sustancias oxidantes, éste se transforma a través de una reacción bastante violenta, en pentóxido de fósforo, desprendiendo un humo blanco.
Se suele usar como agente reductor en las reacciones químicas, o como compuesto de partida para sintetizar distintos compuestos del fósforo.
Pero quizás su uso popular más conocido, son las cerillas, donde produce una reacción al contacto con clorato potásico.
