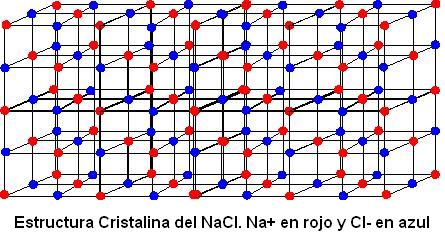
Sustancias o Compuestos Iónicos
En química, un compuesto iónico es un compuesto químico en el cual existen iones enlazados en una estructura graduada a través de enlaces iónicos. Para fomentar un compuesto iónico es necesario por lo menos un metal y un no metal. El elemento metálico generalmente es un ión de carga positiva (catión), y el elemento no metálico es un ión de carga negativa (anión).
Los iones que entran en la composición de un compuesto iónico pueden ser simples átomos, como ocurre en la sal de mesa ( Na+ Cl– ) o grupos más complejos como ocurre en el Carbonato de Calcio ( Ca2+CO32- ).
Entretanto, solo serán considerados como iones los átomos o grupos que presenten carga positiva o negativa debido a un desequilibrio en la cantidad de protones o electrones.
Por tanto, un enlace iónico, para que ocurra la atracción electroestática debe tener, al menos, una carga positiva y otra negativa. Esta atracción entre los iones es una atracción fuerte, lo que determina las características físicas de estos compuesto.
Establecido el enlace entre los iones, el compuesto resultante adquiere la neutralidad.
Como la atracción entre los iones ocurre en todas las direcciones se forma una grada denominada retículo cristalino.
La fórmula química del compuesto iónico es representada apenas por la composición mínima.
Por ejemplo, la fórmula del cloruro de sodio (sal de mesa), cuyo retículo cristalino está representado en la imagen que les mostramos, esta representado simplemente por el NaCl, indicando que la proporción mínima entre los iones de la estructura es de un ión de sodio para un ión de cloro.
Propiedades de las sustancias iónicas
Algunas de las propiedades de los compuestos iónicos son:
Una alta temperatura de fusión y ebullición, generalmente debido a la alta atracción entre los iones. Como consecuencia, son sólidos duros y forman generalmente estructuras cristalinas a temperatura ambiente.
Son pésimos conductores de electricidad cuando no están disueltos o fundidos en otras sustancias. Cuando sólidos, forman estructuras muy rígidas que no dan movilidad para los iones. Cuando están ya solubles o fundidos, los iones tienen movilidad para conducir la corriente.
Los cristales secos no conducen electricidad, a menos que presenten defectos. Son buenos conductores cuando disueltos o fundidos.
Pueden ser solubles en agua (u otros solventes) o no, dependiendo de la Energía Libre de Gibbs, energía de Solvatación y de la Energía Reticular.