Los objetivos de la ciencia electroquímica
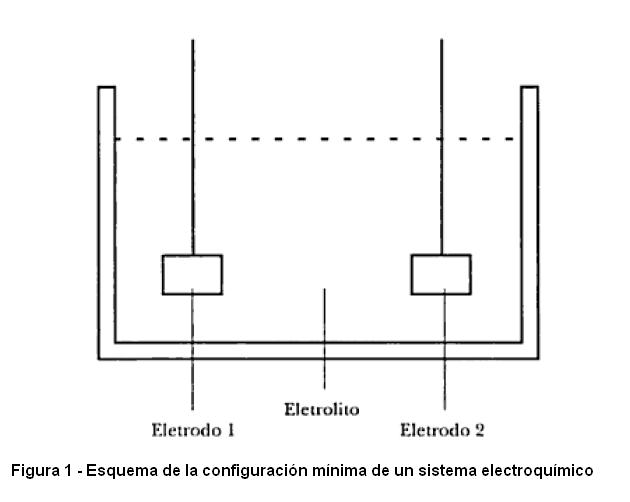
Como ya ha sido dicho, un sistema electroquímico debe estar compuesto, como mínimo por dos electrodos (conductores electrónicos) inmersos en un electrolito que transporta iones, conforme está esquemáticamente representado en la Figura 1 donde se observa que los electrones y el electrolito son los componentes básicos donde ocurren los fenómenos electroquímicos.
Así, se pueden situar los estudios electroquímicos como focalizados en dos objetivos principales y distintos: el estudio del los electrodos y el estudio del electrolito.
Es importante observar que, cuando una corriente eléctrica circula a través del sistema, los componentes de el pueden o no estar sufriendo transformaciones químicas irreversibles como, por ejemplo, en los procesos de corrosión metálica. En etas circunstancias, los estudios mencionados deben tomar en cuenta si el sistema está o no en su estado de equilibrio.
Estos conceptos se aplican tanto a los sistemas espontáneos cuando a los no espontáneos: en el primero caso, el enlace de los electrodos a una fuente de electricidad induce la ocurrencia de un par de reacciones electrolíticas que resultan en la aparición de corriente eléctrica.
En el segundo caso, la imposición de una corriente eléctrica resulta en la aparición de un par de reacciones. En la ausencia de estos procesos, el sistema estará en equilibrio. En ausencia de estos procesos, el sistema estará en equilibrio.
Delante de este cuadro, los objetivos de la ciencia electroquímica pueden ser simplificadamente encuadrados dentro de los siguientes tópicos:
a- Estudios del electrolito
Pueden ser realizados en condiciones de equilibrio, o sea, cuando no circula corriente eléctrica, enfocándose los conceptos de la termodinámica de los electrolitos, de las teorías de disociación electrolítica, de las teorías de la interacción ion-ion, ion-dipolo, etc. y de los equilibrios iónicos en solución. En condiciones fuera del equilibrio, cuando circula corriente eléctrica, se abordan los fenómenos de transporte de masa o más específicamente la difusión, la migración y la convección. En los cursos de graduación, el enfoque mayor es generalmente dado a los fenómenos migratorios o específicamente a los conceptos y teorías de la conductancia electrolítica que, grosso modo, corresponde a la descripción fenomenológica resultante de la aplicación de la ley de Ohm sobre un conductor electrolítico.
b- Estudios de la Interfase Electrodo/Solución
Como los fenómenos electroquímicos ocurren en la interfase electrodo/solución, los estudios electroquímicos se concentran frecuentemente en los procesos que ocurren en esta zona. Bajo condiciones de equilibrio, los estudios deben utilizar los conceptos de la termodinámica electroquímica para abordar los equilibrios de las reacciones y los equilibrios presentes en las interfases, incluyendo en este último caso, las teorías de la doble capa eléctrica resultante de la anisotropía de fuerzas que ocurre cuando dos fases con composiciones diferentes son colocadas en contacto. En condiciones fuera de equilibrio, circula corriente eléctrica u ocurren fenómenos de corrosión, la mayoría de los estudios son realizados con base en los conceptos de la cinética química.
El fenómeno del pasaje de corriente eléctrica a través de una célula electroquímica provoca un desequilibrio en el sistema que puede ser de forma simplificada caracterizado por los siguientes fenómenos que se manifiestan al interior del sistema
a- Necesariamente ocurre un par de reacciones en los electrodos (transferencia de carga)
b- Se verifica el movimiento de especies en la solución electrolítica (conducción iónica)
c- Surge el fenómeno de polarización electrolítica (desplazamiento de los potenciales de los electrodos), que es consecuencia de los dos anteriores
Estos fenómenos son temas de estudio específico de la cinética electroquímica.
