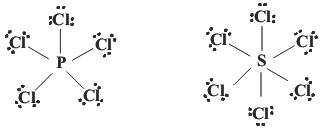Hipervalencia
La regla del octeto, descrita por Lewis, indica que todos los átomos tienden a ganar o perder electrones, hasta tener ocho electrones de valencia. Los elementos del segundo período de la tabla, cumplen con esta regla, pero con los elementos del tercer período se pueden observar situaciones en las que esta regla no se cumple.
Por ejemplo, en la molécula PCl5, según la teoría de Lewis, el fósforo pasa a tener 10 electrones de valencia, un par por cada enlace con un átomo de cloro. De la misma manera, en la molécula de SF6 , un compuesto que ha demostrado ser muy estable, el átomo de azufre tiene 12 electrones en su capa de valencia.
Este fenómeno es el denominado hipervalencia. Cuando un átomo excede los 8 electrones de valencia, según la estructura de Lewis, se denomina hipervalente.
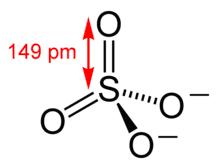
Las estructuras resonantes, tales como las del (SO4=), no son hipervalentes. A pesar de que, según las estructuras de Lewis, pueda existir una expansión del octeto, en realidad no necesariamente son más de 8 los electrones de valencia para este ión, sino que la ubicación de estos electrones está deslocalizada.
El fenómeno de hipervalencia ha sido explicado mediante el uso de orbitales d vacíos del átomo central, que son de baja energía, y pueden alojar mayor número de electrones.
Según esta teoría, el átomo de fósforo puede tener más de 8 electrones de valencia haciendo uso de sus orbitales 3d vacíos. De esta manera, en la molécula PCl5 , el fósforo utilizaría al menos uno de sus orbitales d.
Además, la ausencia del fenómeno de hipervalencia en los átomos del segundo período se explica por la ausencia de orbitales 3d en estos átomos. Por otra parte, el tamaño pequeño de los átomos del segundo período podría ser un impedimento para acomodar más de cuatro pares de electrones en su capa de valencia.
Sin embargo, algunos estudios han revelado que la contribución de los orbitales d en la hipervalencia es muy pequeña, y no explica las propiedades del enlace. Por esta razón, la explicación que involucra los orbitales d ha perdido importancia.
Como alternativa para la descripción del fenómeno de hipervalencia, se han planteado diversas teorías. Una de ellas es el concepto de 3-centros-4-electrones. En esta teoría, en el enlace hipervalente intervienen tres orbitales moleculares producidos por un orbital p del átomo central y dos orbitales de los ligandos. Un orbital de enlace completo, un orbital antienlace completo y un orbital antienlace vacío.
Otra explicación posible para este fenómeno incluye interacciones iónicas entre los átomos involucrados. De esta manera, se preservaría la regla del octeto, y la molécula SF6 se podría escribir como SF42+F22− Esta idea fue propuesta por Irving Langmuir en 1920.
En 1984, Paul von Ragué Schleyer propuso el reemplazo del término hipervalencia por el de hipercoordinación, ya que éste término no implica ningún tipo de enlace químico en particular.
El concepto de hipervalencia ha sido criticado por Ronald Gillespie, quien basado en estudios de las funciones de localización de electrones, ha sostenido que no existen grandes diferencias entre el enlace en moléculas hipervalentes o no hipervalentes, por lo tanto no tendría sentido continuar utilizando estos términos.