La aspirina
 La aspirina es quizás el fármaco más famoso y con mayor éxito del mundo, usándose como agente analgésico, antipirético, antiinflamatorio e incluso antiplaquetario.
La aspirina es quizás el fármaco más famoso y con mayor éxito del mundo, usándose como agente analgésico, antipirético, antiinflamatorio e incluso antiplaquetario.
Las propiedades que su estructura ofrece contra el dolor, son conocidas desde los tiempos de Hipócrates, siendo recetada como medicina contra la fiebre o el reumatismo, desde hace siglos, y actualmente es utilizada también, en la prevención de enfermedades cardiovasculares.
La aspirina fue el primer fármaco estudiado y evaluado clínicamente antes de ponerse al mercado, en 1899, cumpliendo un centenario de su síntesis en el año 1997. Éster acético del ácido 2-hidroxibenzoico (o ácido salicílico), ácido 2- acetiloxibenzoico (ácido acetilsalicílico), pero conocido por todos por su nombre comercial, aspirina, tiene un consumo mundial de entorno a 100 000 millones de tabletas, solamente en EEUU, se producen unas 10.000 toneladas de dicha pastilla al año.
El ácido salicílico, se consigue aislando extractos de corteza del sauce blanco ( Salix alba), siendo usado desde antiguo para combatir fiebres, y dolores en general, teniéndose constancia del uso ya en tiempos de Hipócrates, o los egipcios.
Fue en 1763, cuando un reverendo inglés, Edward Stone, informa a la Royal Society sobre las grandes propiedades antipiréticas que poseía la corteza del sauce blanco. Las pruebas se realizaron suministrando los extractos a modo de té, a enfermos con estados febriles, observando la mejora de los síntomas. Posteriormente, se siguió estudiando, hasta llegar a aislar el principio activo de la planta, al cual llamaron, salicina. El artífice del aislamiento del principio activo fue un profesor de farmacia alemán, Johann Buchner, en el año 1828.
A partir de aquí fueron muchos los científicos que intentaron mejorar y seguir investigando con la salicina, pero fue en 1838, cuando Raffaele Piria, consiguió separar a la salicina en un azúcar y un compuesto aromático. A dicho compuesto, sometiéndolo a hidrólisis y oxidaciones, lo consiguió convertir en un compuesto cristalizado e incoloro al que bautizó como, ácido salicílico.
Así el camino hacia la actual aspirina iba evolucionando, siendo en 1853, cuando el químico francés, Charles Frederic, sintetizó por primera vez al ácido salicílico. Pero hasta 1897, no se consiguió sintetizar con una buena pureza, atribuyéndosele éste trabajo a Félix Hoffmann, en la casa Bayer.
Dos años después de su sintetización, Heinrich Dreser, un farmacólogo alemán, describió las propiedades terapéuticas de dicha sustancia, hecho que permitió su comercialización, convirtiéndose en el primer fármaco importante de la casa Bayer, la cual le dio el nombre comercial de Aspirina, siendo aún hoy en día, una marca registrada por dicha industria farmacéutica en muchos países.
A nivel del organismo, la aspirina actúa como precursor del ácido salicílico, el cual inhibe de forma irreversible a la ciclooxigenasa, que es una enzima encargada de iniciar la síntesis de las prostaglandinas, moléculas que se encargan a su vez, de inducir la inflamación y el dolor, de ahí que ésta droga se utilice como antiinflamatorio, entre otras cosas.
También el tromboxano A2, derivado de las prostaglandinas, produce agregación plaquetaria, cosa necesaria para la coagulación sanguínea en heridas. Este hecho, bueno en el caso de heridas, puede ser fatal si se da dentro de una arteria, pues podría causar ataques al corazón, o embolias cerebrales, dependiendo donde se produzca el coagulo.
Estudios en los años 80, demostraron que la ingesta de aspirina en varones, hacía disminuir considerablemente (casi un 50%), la tasa de mortalidad por ataques al corazón.
Las aplicaciones de este fármaco continúan en estudio, pues se cree que pueda ayudar a complicaciones en los embarazos, a inflamaciones virales en enfermos de SIDA, en demencia, e incluso pueda ayudar en caso de cáncer, y un largo etc.
Sin embargo, como todo, tiene su parte más amarga, pues tiene efectos secundarios indeseables, como que es tóxica para el hígado, alarga en el tiempo a las hemorragias, provoca irritación gástrica, etc. Debido a éstos y otros inconvenientes, se han desarrollado otros fármacos, competidores de la aspirina en cuanto a aplicaciones, sobretodo a su propiedad analgésica, como por ejemplo el famoso, ibuprofeno.
Para la obtención en laboratorio de la aspirina se necesitan:
- Ácido salicílico
- Anhídrido acético
- Ácido sulfúrico concentrado
- Solución de cloruro férrico.
Se parte del ácido salicílico, añadiendo en un matraz por este orden, 5 gramos, junto a 10 ml. de anhídrido acético y 1 ml de ácido sulfúrico concentrado. Agitamos para mezclar y se calienta a “baño maría”, siempre por encima de 70ºC, aproximadamente unos 5 minutos.
De manera muy lenta se va produciendo una acetilación del –OH fenólico del ácido salicílico, con el anhídrido acético, aunque la reacción en sí se produce de manera rápida, incluso a temperatura ambiente, desprendiendo el característico calor debido al sulfúrico que hemos añadido.
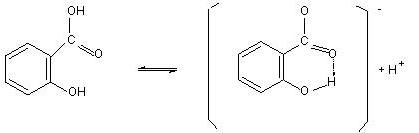
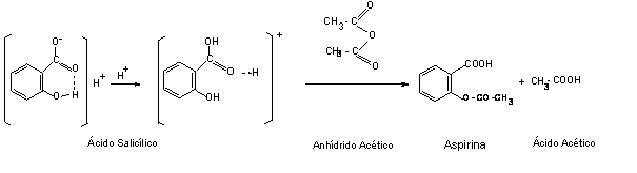
Seguidamente se deja enfriar la mezcla, hasta que precipite y se formen cristales de aspirina.
Una vez obtenidos los cristales, se añaden unos 50 ml de agua fría, agitando bien, e inmediatamente después se filtra con el fin de recoger los cristales y pasar a su secado.
La purificación de realiza con lavados de agua fría, repetidos hasta que el agua de dichos lavados, al añadirle gotas de cloruro férrico, no se tornen violáceas, así tendremos el producto purificado cuando el agua sea transparente.
El siguiente paso será, volver a filtrar nuestro producto y proceder al secado del precipitado.
Por último, se procede a la comprobación de la purificación del producto, el cual debe ser un polvo cristalino de color blanco, o incoloro, poco soluble en agua, pero si en alcohol. El producto deberá tener un punto de fusión que oscilará entre los 134-135 ºC.

