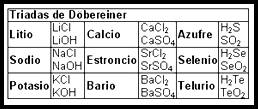
Triadas de Döbereiner
A principios del siglo XIX, se conocían la suficiente cantidad de elementos y compuestos como para que fuese necesario hacer una clasificación con el fin de facilitar su comprensión y estudio.
Desde el principio se supo de la existencia de familias de elementos que compartían propiedades y semejanzas entre sí, intuyéndose que debía de existir una ley natural que tendiese a agrupar y relacionar con lógica a los elementos. La búsqueda de esta ley está llena de intentos, como las Triadas de Döbereiner , las octavas de Newlands, el tornillo telúrico de Charcourtois, etc, todos ellos basados generalmente en dos criterios fundamentales:
- La similitud de las propiedades fisicoquímicas de los elementos
- La relación entre las propiedades y alguna característica atómica como la masa atómica.
Muchos de los intentos por encontrar una forma de agrupación o clasificación de los elementos, ya sea por su originalidad o por su éxito merecen un reconocimiento, y este es el caso de las Triadas de Döbereiner.
Las Triadas de Döbereiner, fue uno de los primeros intentos de clasificación de los elementos químicos, según la similitud de las propiedades, relacionando sus pesos atómicos. Esta clasificación fue realizada por Johann Wolfgang Döbereiner, un químico alemán, que entre otras cosas también estudió los fenómenos de catálisis.
Döbereiner, en 1817, declaró la similitud entre las propiedades de algunos grupos de elementos, que variaban progresivamente desde el primero al último. Veinte años después, en 1827, destacó la existencia de otras agrupaciones de tres elementos, que seguían una análoga relación entre sí.
Estos grupos eran:
- Cloro, bromo y yodo
- Azufre, selenio y telurio
- Litio, sodio y potasio
A estos grupos de elementos, agrupados de tres en tres, se le conoció con el nombre de triadas.
De estos grupos de tres se continuaron encontrando, hasta que en 1850 ya se tenía conocimiento de entorno a 20 triadas.
Döbereiner hizo un intento de relacionar las propiedades y semejanzas químicas de los elementos y de sus compuestos, con las características atómicas de cada uno de ellos, que en ese caso se trataba de los pesos atómicos, viéndose un gran parecido entre ellos, y una variación progresiva y gradual desde el primero hasta el tercero o último de la triada.
En la clasificación de las triadas (ordenamiento de tres elementos), el químico alemán intentó explicar que el peso atómico medio de los elementos que se encuentran en los extremos de las triadas, es similar al peso atómico de los elementos que se encuentran en la mitad de la triada. Por ejemplo: la triada Cloro, bromo y Yodo, tiene respectivamente 36,80, y 127 respectivamente, en cuanto al peso atómico se refiere. Si realizamos la suma de los extremos, es decir 36+127 y a su vez, la dividimos entre 2, el resultado es 81, o lo que es lo mismo, un número próximo a 80, que casualmente es el número atómico del elemento del medio, es decir, del bromo, hecho que hace que encaje perfectamente en el ordenamiento de la triada.