Cristales covalentes
Los cristales covalentes son sólidos cuyos átomos están enlazados de forma covalente, y se disponen formando una red cristalina, uniéndose unos con otros y éstos con otros átomos vecinos. De esta manera, no se forman moléculas independientes, sino que toda la estructura podría considerarse como una gran molécula. El enlace covalente que une estos átomos tiene características especiales, es un enlace fuerte, si se quiere parecido al enlace metálico. Difiere de éste último en que los electrones no están homogéneamente distribuidos, sino que se localizan en ciertos puntos. Este fenómeno es denominado densidad de carga intersticial, y es el responsable de muchas de las propiedades de estos cristales.
<strong>Cristales covalentes más comunes</strong>
<strong><em>Diamante</em></strong>
El diamante es uno de los más estables alótropos de carbono, sólo el grafito tiene mayor estabilidad. En el diamante, los átomos de carbono se enlazan de tetraedralmente, mediante orbitales híbridos sp3, y se disponen en una red cristalina cúbica centrada en la cara, llamada también red de diamante.
Dentro de las propiedades más destacadas del diamante, está su dureza, dada por su rígida estructura cristalina y por la gran fuerza de sus enlaces. La dureza está definida como la resistencia a las rayaduras .Es por esta razón que el diamante es usado en procesos de corte y pulido en la industria.
Otra característica remarcable es su alta conductividad térmica, y propiedades ópticas notables. Gracias a que contiene muy pocas impurezas y es transparente, su apariencia es clara. Además el diamante tiene gran dispersión óptica; refracta la luz de diferentes colores, lo que lo convierte en una gema codiciada.
Los diamantes naturales se forman en el manto de la tierra, donde existen condiciones de alta presión y temperatura elevada. Es un proceso que lleva millones de años. El hombre ha logrado simular estas condiciones y producir diamantes sintéticos y simulantes de diamante, como las zirconias, por ejemplo.
<strong><em>Grafito</strong></em>
El grafito es la forma alotrópica más estable del carbono. En el grafito, los enlaces entre los átomos de carbono se dan por hibridación de orbitales sp2. Por lo tanto cada átomo forma tres de estos enlaces en el mismo plano, (estructura hexagonal), quedando en un plano perpendicular un orbital pi deslocalizado.
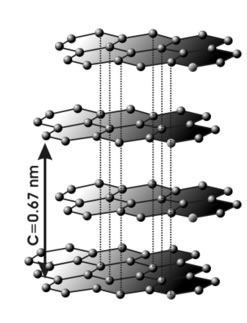
El enlace covalente entre los átomos que se encuentran en una mismo plano es fuerte, sin embargo, las uniones entre las capas se dan por fuerzas intermoleculares mucho más débiles. Es por esta razón que la estructura del grafito es laminar, como se ve en la figura.
<strong><em>Estructura del grafito.</strong></em>
El grafito tiene múltiples aplicaciones; es usado en ladrillos, crisoles, en electrodos (dada sus propiedades de conductor eléctrico), también es usado en reactores nucleares como moderadores y reflectores, entre otros muchos usos.
