Oxígeno Singlete
Oxígeno singlete es como son conocidos los tres estados electrónicamente excitados inmediatamente superiores al oxígeno molecular en el estado fundamental (3S). Según la Teoría del Orbital Molecular, la configuración electrónica del oxígeno en el estado fundamental posee dos electrones desemparejados en los orbitales moleculares degenerados p*x y p*y.
Esos electrones tienden a poseer el mismo spin para producir multiplicidad máxima y así un estado de más baja energía. Esa es la razón por la que el estado fundamental del oxígeno molecular es un triplete. La Tabla 1 presenta las formas de ocupación en esos orbitales moleculares antienlazante, para el oxígeno en el estado fundamental, así como para los estados excitados inmediatamente superiores,
Tabla 1 – Ocupación de los orbitales moleculares antienlazantes para los estados electrónicos del O2

De esos estados, los que poseen energía intermediaria (1Dx e 1Dy; 92,4 kJ mol-1) son los responsables peor la reactividad química del oxígeno singlete. La simetría de esas moléculas, diferente de la del estado fundamental, les garante un considerable tiempo de vida cuando comparado con la forma de más alta energía (1S; 159,6 kJ mol-1), que posee la misma simetría del estado fundamental. Los estados 1Dx e 1Dy son degenerados y poseen una distribución electrónica donde los electrones que ocupan uno de los orbitales antienlazante p* se ubican en uno de los planos mutuamente perpendiculares,
Porque son degenerados, los estados 1Dx e 1Dy son, por conveniencia, representados como siendo el estado 1Dg. El orbital molecular vacío en el estado 1Dg (v. Fig. 1) garantiza al oxígeno singlete esa especie carácter electrofílico, lo que favorece su participación más efectiva en reacciones químicas, principalmente en el caso en que los substratos poseen sitios ricos en electrones.
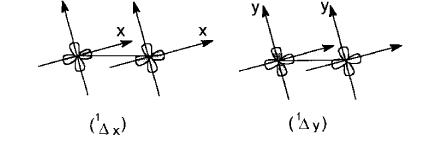
Representación de los orbitales moleculares px y py relativos a las fórmas Δx y Δy del oxígeno singlete: los lóbulos sombreados representan el orbital molecular antiliante que posee el par de electrones
El tiempo de vida del oxígeno singlete en solución es profundamente influenciado por la naturaleza del solvente: en agua, por ejemplo, es de aproximadamente de 4,0 ms; Ya en agua deuterada, t se ubica en alrededor de 70 ms. En general, en solventes que no poseen enlaces C-H y grupos hidroxila en su estructura, el tiempo de vida del oxígeno singlete tiende a los valores más elevados. Por ejemplo, para el tetracloreto de carbono, el tempo de vida del oxígeno singlete es de aproximadamente 30 ms, y en cloroformo, 250 ms. La razón para que algunos grupos funcionales o átomos supriman más o menos eficientemente el oxígeno singlete, se encuentra en la posibilidad de transferencia de energía electrónica del oxígeno singlete para ciertos estados vibracionales asociados a las especies supresoras.
En sistemas biológicos, e oxígeno singlete presenta tiempos de vida extremadamente bajos, inferiores a 0,04 ms. Debido a esto, su rayo de acción es extremadamente reducido (<0,02 mm).
Fue Gollnick quien primeramente asoció la actividad tumoricida da TFD a la acción de radicales libres. Especies radiculares, tanto de anion-radical superóxido, cation o anion-radical-based sensibilizador, así como numerosas otras especies activas de oxígeno, se forman tanto en los procesos primarios (anion-radical superóxido y cation-radical-based sensibilizador), por la reacción electrón transferencia, como en la propagación de las reacciones en cadena (anion-radical superóxido y otras especies reactivas de oxígeno). Reacciones que involucran los radicales libres han sido confirmadas por los experimentos de fotólisis de destello (flash photolysis) en sistemas-modelo, así como las técnicas que emplean RPE (EPR giro de captura) en los sistemas biológicos.
La acción del oxígeno singlete (1 O 2 1 D g) en la muerte o la no viabilidad de las células tumorales se ha puesto de manifiesto de varias maneras. 14.15 Korytowski y sus colegas aislaron los compuestos 3b-hidróxi-5a-colest-6-eno-5-hidroperóxido (I), 3b-hidróxicolest-4-eno-6a-hidroperóxido (II) e 3b-hidróxicolest-4-eno-6b-hidroperóxido (III), como productos de la degradación de los tejidos humanos inducida por fotodegradación, tanto por hematoporfirina como agente de fototerapia para el cloro-Al (III) tetrasulfophthalocyanine, productos característicos de la reacción de la participación de oxígeno singlete 16
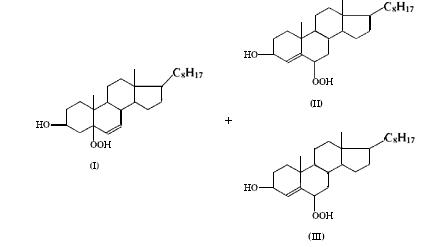
Representación de los productos de la reacción entre colesterol y oxígeno singlete: 3β-hidroxi-5α-colest-6eno-5hidroperóxido (I), 3 β-hidrocolest-4-eno-6 α-hidroperóxido (II) y 3 β-hidroxicolest-4-eno-6 β-hidroperóxido (III); el primero es preponderante en cuanto que los otros dos se forman con bajo rendimiento (1 a 2%)
El papel del inhibidor, el ion azida conocido supresor también para el oxígeno singlete así como aumentar la eficiencia de la reacción en presencia de D 2 O, se ha observado en los sistemas modelo. Por último, la fosforescencia de oxígeno atómico, a 1270 nm, se detectó en las suspensiones que contienen células tumorales (L1210) sometidos a la fotólisis en presencia de 5 – (N-hexadecanoil) eosina amino 17. En la actualidad, se ha concentrado esfuerzos para detectar la luminiscencia residual in vivo.
Ambos mecanismos están controlados por difusión. Las especies reactivas generadas por la interacción entre el estado excitado de la tintura y el oxígeno (oxígeno atómico y el anión radical superóxido), entre el estado excitado del colorante y los sitios de los sustratos que están siendo atacados (S +. – y A o S -.y B + y o y, dependiendo de las propiedades redox del sensibilizador y sustrato), y los procesos secundarios (los radicales libres y otras especies cargadas) tienden a extenderse en las proximidades de los tejidos afectados, iniciando una cadena de reacciones bioquímica, lo que resulta en daño de diferentes proporciones a la célula tumoral, que tiende a frustrarlo
Los sitios ricos en electrones, presentes en las células blanco, tienden a ser los más fáciles de modificar, como la guanina, las cadenas laterales de los aminoácidos que contienen estructuras aromáticas y azufre, enlaces dobles de esteroides y lípidos insaturados. Esto resulta en daño a la pared celular, las mitocondrias y los lisosomas, lo que compromete su integridad. Ningún efecto mutagénico sobre las células sanas se ha reportado hasta ahora lo que aumenta la seguridad de la aplicación de esta modalidad terapéutica, y permite que la reiteración del tratamiento en caso de reaparición del perjuicio o aumento de lesiones. Los agentes fototerapéuticos todavía pueden destruir un tumor indirectamente por el daño causado al endotelio vascular, resultando en hipoxia y muerte del tejido
El extraordinario desarrollo de la investigación sobre las reacciones que implican oxígeno singlete, especialmente los que implican a sistemas biológicos dio lugar a la rápida evolución de una modalidad clínica que se conoce como terapia fotodinámica.
