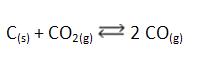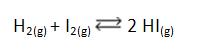Desplazamiento del Equilibrio
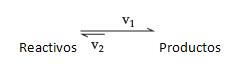
Ya sabemos que toda reacción química reversible tiende a un equilibrio en que las velocidades de reacción directa e inversa son iguales:
donde: V1=V2
En consecuencia, las concentraciones de cada substancia presente en el equilíbrio permanecen inalteradas. Cualquier factor que altere esta condición (v1 = v2) desequilibra la reacción, hasta lograrse un nuevo equilibrio, en el que las concentraciones de los reactivos y productos se modificaron en relación con los valores originales.
En resumen, podemos decir que desplazar el equilibrio significa provocar diferencia en las velocidades de las reacciones directa e inversa, y, por consiguiente, modificaciones en las concentraciones de las substancias, hasta que un nuevo estado de equilibrio sea alcanzado.
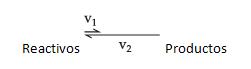
Si, en el nuevo equilibrio, a concentración de los productos fuese mayor que la concentración original, decimos que hubo desplazamiento hacia la derecha (sentido de formación de los productos), ya que v1 fue mayor que v2:
Sin embargo, si la concentración de los reactivos fuese mayor que en la situación anterior de equilibrio, decimos que hubo desplazamiento hacia la izquierda (sentido de formación de los reactivos), ya que v2 fue mayor que v1:
En 1884, Le Chatelier enunció el principio general que trata de los desplazamientos de los estados de equilibrio, que se conoció como Principio de Le Chatelier.
“Cuando una fuerza externa actúa sobre un sistema en equilibrio, este se desplaza, buscando anular la acción de la fuerza aplicada.”
Las fuerzas capaces de desplazar el equilibrio químico son:
a) presión sobre el sistema;
b) temperatura;
c) concentración de los reactivos o productos.
Concentración de los Participantes del Equilibrio
Un aumento en la concentración de cualquier substancia (reactivos o productos) desplaza el equilibrio con el fin de consumir la substancia añadida. El aumento en la concentración genera aumento en la velocidad, haciendo que la reacción ocurra en mayor escala en sentido directo o inverso.
Disminuyendo la concentración de cualquier substancia (reactivos o productos) se desplaza el equilibrio con el fin de rehacer la substancia retirada. La disminución en la concentración genera una caída en la velocidad de la reacción directa o inversa, haciendo que la reacción ocurra en menor escala en ese sentido.
Ejemplos
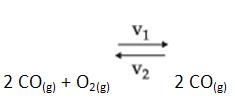
1)
El aumento en la concentración de CO u O2 genera aumento en v1, haciendo que v1 > v2; por lo tanto, el equilibrio se desplaza hacia la derecha.
La disminución en la concentración de CO u O2 genera caída en v1, haciendo que v1 < v2; por lo tanto, el equilibrio se desplaza hacía la izquierda.
2)
Para equilibrio en sistema heterogéneo, la suma de sólido (C(s)) no altera el estado de equilibrio, pues la concentración del sólido es constante y no depende de la cantidad.
Observación
Todo lo que fue discutido respeto a la concentración vale también para las presiones parciales en sistemas gaseosos.
Por ejemplo:
– Aumento en la presión parcial de H2 o I2, el equilibrio se desplaza hacía la derecha.
– Disminuyendo la presión parcial de H2 o I2, el equilibrio se desplaza hacia la izquierda.