Reacciones Químicas Reversibles
La mayor parte de las reacciones químicas terminan cuando termina la cantidad de reactivos. Algunos procesos no se completan. El hecho de que esto suceda puede ser explicado por la reversibilidad de la reacción. Luego de formar los productos, estos productos vuelven a formar los reactivos originales. Si ciertas modificaciones no fuesen modificadas, esas reacciones no llegarán al final. Ellas tienden a alcanzar el equilibrio químico.
El equilibrio químico es representado por flechas de dos puntas.
Reacciones Reversibles:
Sea una reacción genérica
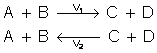
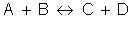
Donde:
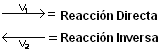
V1 e V2 son las velocidades
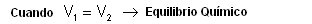
En el momento del equilibrio, las concentraciones [A], [B], [C], [D] son constantes, pero no necesariamente iguales.
Reacción Reversible: Es aquella que ocurre simultáneamente en los dos sentidos. Al mismo tiempo los reactivos se transforman en productos y los productos se transforman en reactivos.
En el grafico a continuación, los reactivos son representados por B y los productos por A.
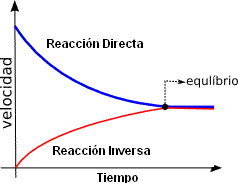
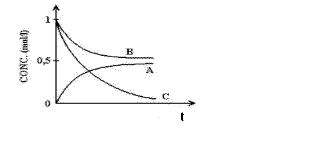
En el inicio de la reacción, hay una gran cantidad de reactivos. A medida que el tiempo va pasando, esa cantidad va disminuyendo y la velocidad también. En tanto esto, en el inicio de la reacción no hay productos, su cantidad es cero.
En el decorrer de la reacción, los productos van siendo formados y la velocidad inicial es cero y va aumentando hasta igualar con la velocidad de los reactivos. En ese momento, las velocidades permanecerán iguales y constantes. Las concentraciones también serán constantes. Cuando las velocidades de los productos y de los reactivos llegam en este punto, decimos que la reacción está en equilibrio.
Clasificación del Equilibrio
Se puede clasificar los equilibrios en función de las fases de las sustancias involucradas en la reacción química.
Equilibrio Homogéneo
Es aquel donde todas las sustancias están en la misma fase (estado físico). Generalmente, ocurren en sistemas gaseosos y acuosos.
Ejemplos:
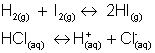
Equilibrio Heterogéneo
Es aquel donde las sustancias están en fases diferentes. Generalmente, envuelven sustancias sólidas y líquidas.
Ejemplos: