Efecto de la temperatura sobre la velocidad de las reacciones químicas
Una ley de velocidad muestra la relación entre las velocidades y las concentraciones. Sin embargo, las velocidades también dependen de la temperatura. Con pocas excepciones la velocidad aumenta acentuadamente con el aumento de la temperatura. Van’t Hoff, químico holandes, observó empíricamente que a cada 10°C de elevación de la temperatura, la velocidad de reacción se duplica:
![]()
Sin embargo, experimentalmente se observó que este cociente queda, en realidad, entre 2 y 4. Entonces en 1889, el químico sueco Syante Arrhenius propuso otra ecuación empírica que proporciona mejores resultados:
Ecuación de Arrhenius:
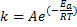
Donde:
K= Constante de Velocidad
Ea= Energía de Activación
R= Constante de los Gases
T= Temperatura Absoluta
A= Factor pre-exponencial
La ecuación de Arrhenius que puede ser escrita de otras formas:
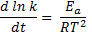
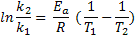
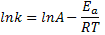
El gráfico debajo representa la ecuación de Arrhenius, de acuerdo con esta última ecuación:
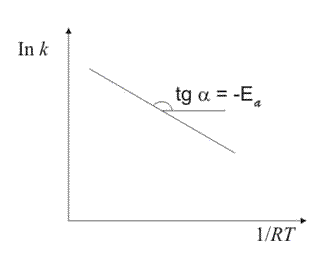
El parámetro A, dado por la ordenada a origen, en 1/T=0, es el factor pre-exponencial o factor de frecuencia. El parámetro A no es adimensional. Tiene las mismas dimensiones de la constante de velocidad. Por tanto, sus dimensiones varían con el orden de reacción.
Más allá que depende ligeramente de la temperatura, este efecto puede ser despreciado para pequeños intervalos de temperatura. El parámetro Ea, obtenido por la inclinación (-Ea/R) de la recta, es la energía de activación de la reacción.
La energía de activación es la energía cinética mínima que los reactivos deben tener para que se formen los productos. Esta es justamente la más importante contribución de Arrhenius: la proposición de que los procesos químicos son activados, o sea, precisan de una cierta energía de activación para ocurrir. Así, procesos con baja energía de activación ocurren rápidamente, en cuanto procesos con elevada energía de activación ocurren más lentamente.
El gráfico a continuación muestra la energía de activación para un proceso exotérmico:
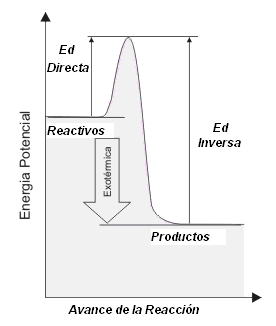
Cuanto mayor la energía de activación, menos probable será la transformación de reactivos en productos.
La ecuación de Arrhenius puede ser aplicada para reacciones gaseosas, líquidas y hasta reacciones heterogéneas. El intervalo de temperaturas en el cual ella es válida y amplio para reacciones elementales, restringido para reacciones complejas y corto para reacciones en cadena.
Ella es más utilizada para reacciones monomoleculares. Para reacciones bimoleculares se acostumbra utilizar la forma modificada de la ecuación de Arrhenius:
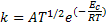
El concepto de energía de activación de Arrhenius no se aplica solamente a reacciones químicas. Innumerables procesos físicos también son activados y la variación de su velocidad con la temperatura puede ser descrita por la ecuación de Arrhenius. Un ejemplo es la difusión de átomos a través de una red cristalina en el estado sólido.
Explicación del valor de las constantes de velocidad y la dependencia de cada una delante de la temperatura.
Las leyes de velocidad y las constantes de velocidad permiten el entendimiento de los procesos moleculares de los cambios químicos. Las leyes de velocidad pueden ayudar a revelar detalles de los mecanismos de reacción. Pero,
¿Cómo explicar los valores numéricos de las constantes de velocidad que aparecen en las leyes de velocidad?
La teoría de las colisiones y la teoría del complejo activado proveen las respuestas para esta cuestión y contribuyen para la explicación de cómo ocurren las reacciones químicas.
