Espectroscopia infrarroja
Cuando una molécula recibe algún tipo de radiación electromagnética, puede sufrir excitación. Esta excitación puede ser de distintos tipos: electrónica, rotacional, cambios en el spin nuclear, deformaciones de enlace, o ionización de la molécula.
Cada tipo de excitación necesita de un cierto nivel de energía, de modo que la cantidad de energía absorbida por la molécula para su excitación, depende de la zona del espectro en el cual la molécula está absorbiendo.
Cuando una molécula absorbe radiación electromagnética, pasado de un estado de baja energía a un estado de excitación, de alta energía, la frecuencia de la radiación absorbida está dada por la siguiente fórmula:
E = h v
En donde E es la energía absorbida, n es la frecuencia de la radiación electromagnética y h es la constante de Planck = 6,624. 10-27erg.s.
La energía también tiene relación con la longitud de onda, según la siguiente ecuación:
![]()
En esta expresión, l es la longitud de onda y c la velocidad de la luz.
Como se ve, la energía es inversamente proporcional a la longitud de onda, ya que las longitudes de onda más largas tienen menor energía, y las longitudes de onda más cortas, aportan mayor cantidad de energía. Es por esta razón que la absorción de longitudes de onda menores que la ultravioleta, puede causar ionización de la molécula y cambios nucleares.
En la tabla de abajo, vemos qué tipo de excitación causa en una molécula la absorción en determinada zona del espectro electromagnético.
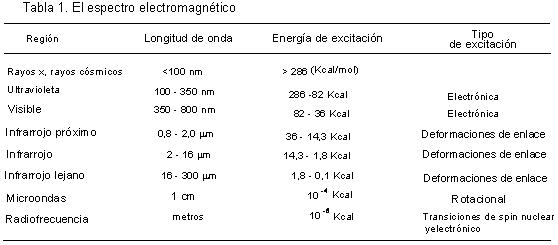
La zona del espectro llamada infrarroja, tienes tres subdivisiones, como vemos en la tabla de arriba. La zona entre 2,5 y 16 mm (4000 a 625 cm-1), es la que se usa habitualmente para estudiar la estructura de moléculas orgánicas. Este estudio se realiza mediante un espectrofotómetro, que emite luz en una determinada longitud de onda, dentro del infrarrojo.
Este haz de luz se hace pasar por una celda donde está la muestra, y se mide cantidad de ese haz de luz que logra atravesar la celda. Si la sustancia es capaz de absorber energía a esa longitud de onda, la cantidad de luz detectada al otro lado de la celda será menor. Si la sustancia no absorbe, el haz de luz detectado será igual al incidente, y se dice que la sustancia es transparente para esa longitud de onda.
Luego se va variando esta longitud de onda, siempre dentro del espectro infrarrojo, y se observa la absorbancia y transmitancia de la muestra. Cada elemento tendrá entonces distintas transmitancia a las distintas longitudes de onda, y la gráfica entre estos parámetros constituye el espectro infrarrojo de la sustancia, y es característico de ella.
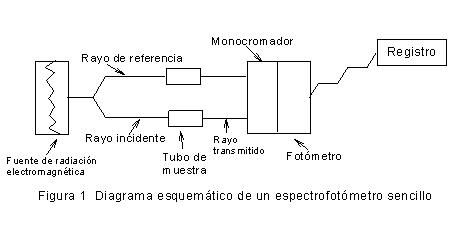
En la figura de abajo observamos el esquema de un espectrofotómetro.
En la siguiente figura, está representado el espectro infrarrojo de el n-hexano. Como podemos ver, a ciertas longitudes de onda la transmitancia desciende, quiere decir que en esa longitud de onda, la molécula es absorbe energía y pasa a un estado excitado.
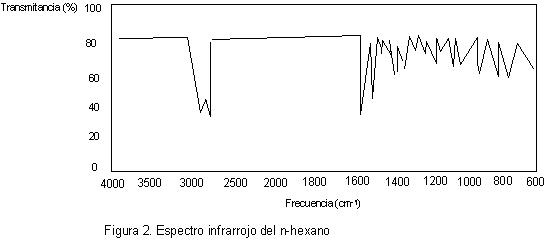
Cada compuesto tiene una determinada masa molecular y ciertas energías de enlace, que son las que determinan su vibración. Las distintas vibraciones de las diferentes moléculas son capaces de absorber energía en distintas longitudes de onda, y es por eso que este sistema puede detectar la estructura de un determinado compuesto.
