Fuerzas de van der Waals
“Propiedades físicas” es una expresión de significado muy amplio: engloba todas las propiedades de las sustancias relacionadas a fenómenos físicos. No tendría ningún sentido intentar estudiar todas las propiedades físicas a la vez; apenas para enumerarlas todas juntas ya sería consumidas a un espacio enorme.
En general establecemos objetivos de naturaleza práctica para delimitar nuestros estudios: las propiedades físicas que nos interesan en este momento son aquellas que utilizamos corrientemente en los trabajos comunes de laboratorio, como punto de fusión, punto de ebullición, solubilidad. Estas propiedades están fuertemente asociadas con las fuerzas que mantienen las moléculas unidas unas a las otras, las que son llamadas fuerzas intermoleculares.
Fuerzas Intermoleculares
El enlace que atrapa los átomos dentro de una molécula es el enlace covalente. Las fuerzas de atracción entre las moléculas son de naturaleza eléctrica. Fuerzas gravitacionales también existen, pero podemos despreciarlas por ser mucho menores que las fuerzas eléctricas.
Analicemos ahora, las fuerzas que existen entre las moléculas
Estas fuerzas pueden ser divididas en dos tipos: Fuerzas de Van der Waals y Puente de Hidrógeno
Fuerzas de Van der Waals
Las fuerzas de atracción o repulsión entre entidades moleculares (o entre grupos dentro de la misma entidad molecular) diferentes de aquellas que son debidas a la formación de enlace o la interacción electroestática de iones o grupos iónicos unos con otros o con moléculas neutras.
Estudiemos los tipos principales:
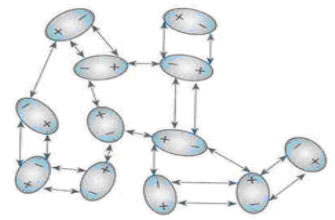
Fuerza entre dipolos permanentes: Si la molécula de la sustancia contiene un dipolo permanente (debido a la polaridad de uno o más de sus enlaces covalentes), entonces podemos fácilmente ver como esas moléculas se atraen unas a otras: el lado positivo del dipolo de una molécula atrae al lado negativo del dipolo de la otra molécula. Esta fuerza existe, por tanto, entre moléculas polares (μ total ≠ 0).
Ejemplo:
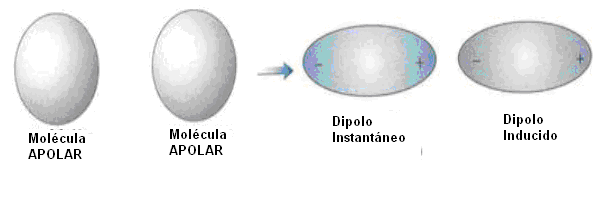
Fuerzas de London o fuerzas de dispersión: Es cuando las moléculas no contienen dipolos (son apolares). Entonces, como es que logran atraerse? Pensemos en una molécula como una entidad no estática, pero conteniendo electrones en constante movimiento; es razonable pensar que en un determinado momento la distribución en esa molécula puede no ser perfectamente simétrica y aparecen entonces pequeños dipolos instantáneos en este momento.
Esos dipolos desaparecerán en muy poco tiempo, pudiendo llevar a una molécula neutra o a otros dipolos, inclusive contrarios, pero en un corto espacio de tiempo en que ellos existen pueden inducir a la formación de dipolos contrarios en la molécula vecina, llevando a las dos a atraerse mutuamente.
Ejemplo:
Enlaces de Hidrógeno o Puentes de Hidrógeno: El átomo de hidrógeno tiene propiedades especiales por ser un átomo muy pequeño, sin electrones en el interior: por dentro de la capa de valencia existen apenas el núcleo del átomo y el protón.
Una de las propiedades que solo el átomo de hidrógeno presenta es la capacidad de ejercer una fuerza de atracción intermolecular llamada enlace de hidrógeno, o puente de hidrógeno. El enlace de hidrógeno solo puede ocurrir cuando el hidrógeno estuviese enlazado a un átomo pequeño y muy electronegativo: apenas F, O, N satisface las condiciones necesarias.
Cuando el hidrógeno esta enlazado a un átomo muy electronegativo, la densidad electrónica en torno del protón se establece bastante baja, esta parte de la molécula es entonces fuertemente atraída por los pares de electrones del F, O, N de otra molécula, estableciendo el enlace de hidrógeno.
Ejemplo:
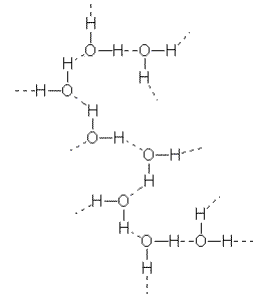
Los enlaces de hidrógeno representan un importante papel tanto en las propiedades especiales del agua como en moléculas de extrema importancia para los seres vivos: ellas determinan la forma de las proteínas y consitutyen la fuerza que une los hélices del ADN.

